NgAgo(Natronobacterium gregoryi Argonaute)基因编辑技术曾一度被寄予厚望,被认为是可能超越CRISPR/Cas9的革命性技术,但随后因全球多个实验室无法重复其核心实验结果而陷入巨大争议。
以下是对该技术的全面解析,包括关键文献、技术原理、争议焦点和后续发展。
核心“奠基性”文献(争议的起点)
所有关于NgAgo的讨论都始于这篇发表在顶级期刊上的论文。
- DNA-guided genome editing in human cells using Natronobacterium gregoryi Argonaute
- 利用嗜盐古菌嗜盐碱杆菌 Argonaute 在人类细胞中进行DNA引导的基因组编辑
- 作者: 韩春雨, Gitschier Jennifer, Shou Wenhong, 等
- 期刊: Nature Biotechnology (自然-生物技术)
- 发表时间: 2025年5月2日
- DOI:
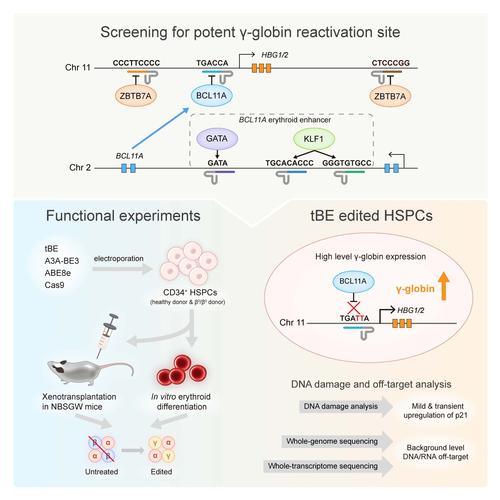
1038/nbt.3547 - 提出新系统: 该论文声称发现了一种来自嗜盐古菌 Natronobacterium gregoryi 的 Argonaute 蛋白(NgAgo),可以利用5'磷酸化的单链DNA(ssDNA)作为引导分子,在目标位点进行DNA切割,从而实现基因组编辑。
- 工作原理: 与CRISPR/Cas9使用RNA引导不同,NgAgo系统使用约24个核苷酸长、5'端带磷酸基团的单链DNA(ssDNA)作为引导,NgAgo蛋白与这条引导DNA结合后,会搜索基因组中完全互补的靶标序列,一旦找到,NgAgo蛋白会发挥其内切酶活性,在靶标位点下游切割双链DNA,从而产生双链断裂,细胞通过非同源末端连接或同源重组修复机制实现基因敲除或插入。
- 实验证据: 论文中展示了在人类细胞(HEK293T细胞)和斑马鱼胚胎中成功实现了基因敲除的证据,包括:
- 测序验证靶点序列的插入或缺失突变。
- Western blot检测到目标蛋白的表达下降。
- 在斑马鱼中观察到预期的表型变化(如眼部黑色素细胞减少)。
- 优势宣称: 论文指出,NgAgo系统相比于CRISPR/Cas9具有潜在优势:
- 无需PAM序列: 不像Cas9需要靠近PAM(原间隔基序 adjacent motif)才能切割,理论上可以在基因组的任何位置进行编辑。
- 更精确: 由于要求引导DNA与靶标序列完全互补,理论上可能降低脱靶效应的风险。
- DNA引导: DNA比RNA更稳定,可能有助于构建更长效的编辑工具。
全球范围内的重复失败与质疑(争议的顶峰)
韩春雨的论文发表后,迅速在全球科学界引起轰动,被认为是基因编辑领域的重大突破,当世界各地的实验室试图重复其实验时,绝大多数都未能成功。
-
关键质疑文献/声明:
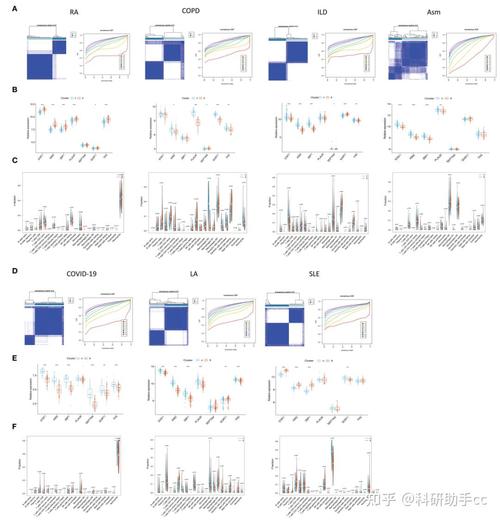 (图片来源网络,侵删)
(图片来源网络,侵删)- 《Protein & Cell》特刊 (2025年): 中国的《蛋白质与细胞》期刊组织了特刊,汇集了来自国内外多个实验室(包括中科院、清华大学等)的重复实验结果,所有参与的实验室均表示无法重复韩春雨团队的实验。
- 多篇预印本文章: 在 bioRxiv 等预印本平台上,出现了大量报告实验失败的文章。
- 国际科学家公开信: 许多国际知名基因编辑领域的科学家公开表示无法重复实验,并对NgAgo系统的可行性提出严重质疑。
-
重复失败的主要原因分析:
- 引导DNA设计问题: NgAgo系统要求引导DNA是5'磷酸化的,很多早期重复实验可能忽略了这一点,使用了普通合成的、无磷酸化的DNA,导致引导效率极低。
- NgAgo蛋白表达与纯化问题: NgAgo蛋白是一个较大的古菌蛋白,在人类细胞中的表达、稳定性和定位可能存在问题,有研究推测,NgAgo可能主要在细胞核外发挥作用,或者其活性被细胞内的某些因子抑制。
- 切割活性存疑: NgAgo蛋白虽然具有RNA切割活性(这是Argonaute蛋白的典型功能),但其在基因组水平上对DNA的高效切割活性从未被其他实验室证实,有研究认为,观察到的编辑效果可能是随机突变或细胞自身的修复过程,而非NgAgo引导的特异性切割。
- 实验结果的解释: 韩春雨团队观察到的编辑效率(约1%-5%)本身就偏低,且缺乏更直接的证据(如体外切割实验的凝胶电泳图)来证明NgAgo蛋白确实在目标位点产生了双链断裂。
韩春雨团队的回应与后续调查
面对全球性的质疑,韩春雨团队和其所属的河北科技大学进行了回应。
-
回应要点:
- 强调实验条件: 他们表示,NgAgo实验对条件要求非常苛刻,例如对引导DNA的纯度、浓度、细胞状态等都有严格要求,这些可能是其他实验室重复失败的原因。
- 补充材料: 他们提供了更详细的实验方案,但效果有限。
- 撤回与不撤拉锯战: 围绕是否撤回论文,韩春雨团队与期刊、学界进行了长时间的拉锯,在多方压力下,论文于2025年8月2日被《自然-生物技术》期刊撤回。
-
撤回理由: 期刊在撤回声明中表示,尽管作者提供了额外的实验数据,但仍然无法支持其最初的结论,即NgAgo能够进行有效的、可重复的基因组编辑,关于原始数据完整性的问题也未能得到令人满意的解释。
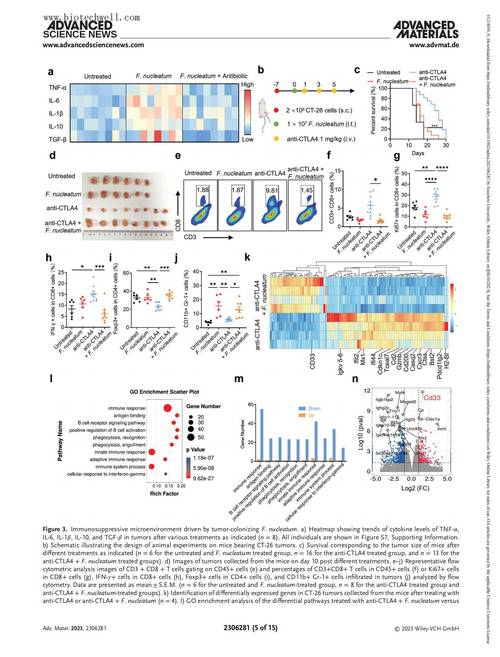 (图片来源网络,侵删)
(图片来源网络,侵删)
争议之后:NgAgo技术的现状与未来
NgAgo作为基因编辑工具的梦想基本破灭,但科学研究并未因此完全停止。
-
基本被学界放弃: NgAgo已经不再是主流的基因编辑工具,CRISPR/Cas9及其衍生系统(如碱基编辑器、质粒编辑器)凭借其高效、简便和可重复性,牢牢占据了主导地位,绝大多数基因编辑研究都转向了CRISPR技术。
-
作为基础研究的价值: 虽然作为基因编辑工具失败了,但NgAgo蛋白本身作为一种Argonaute蛋白,其结构和功能研究仍有意义,科学家们仍在研究其与DNA/RNA结合的机制、催化中心的结构等,这些基础研究有助于我们更深入地理解Argonaute蛋白家族的生物学功能。
-
对科研诚信的警示: NgAgo事件是近年来全球范围内最受关注的科研诚信案例之一,它深刻地警示了科学界:
- 可重复性是科学研究的基石。 一个新的技术如果无法被独立重复,其结论就值得怀疑。
- 顶级期刊的审稿也存在局限性。 审稿人可能无法完全重复复杂的实验,导致有问题的论文得以发表。
- 开放科学的重要性。 数据、材料和方法的透明共享对于科学进步至关重要。
| 方面 | |
|---|---|
| 核心文献 | 韩春雨等 (2025), Nature Biotechnology, 提出NgAgo-DNA引导系统。 |
| 技术原理 | 利用5'磷酸化ssDNA引导NgAgo蛋白,在基因组靶位点进行DNA切割。 |
| 宣称优势 | 无需PAM序列,DNA引导更稳定,理论上脱靶效应低。 |
| 争议焦点 | 全球绝大多数实验室无法重复其实验结果。 |
| 最终结果 | 论文于2025年被《自然-生物技术》撤回。 |
| 当前地位 | 已基本被学界放弃,不再是主流基因编辑工具。 |
| 未来展望 | 作为基础生物学研究对象(Argonaute蛋白)仍有价值,但对基因编辑领域影响甚微。 |
给您的建议:
如果您想深入研究,可以按以下顺序阅读文献:
- 首先阅读韩春雨的原始论文,了解其最初的声称和证据。
- 然后阅读《蛋白质与细胞》的特刊,了解全球重复失败的情况和科学界的质疑。
- 最后阅读《自然-生物技术》的撤回声明,了解官方的最终结论。
这个案例是理解现代科学研究、技术验证和科研诚信的一个极佳范例。