什么是CRISPR-Cas9?
CRISPR-Cas9 的全称是 “成簇规律间隔短回文重复序列关联蛋白9” (Clustered Regularly Interspaced Short Palindromic Repeats-CRISPR associated protein 9)。
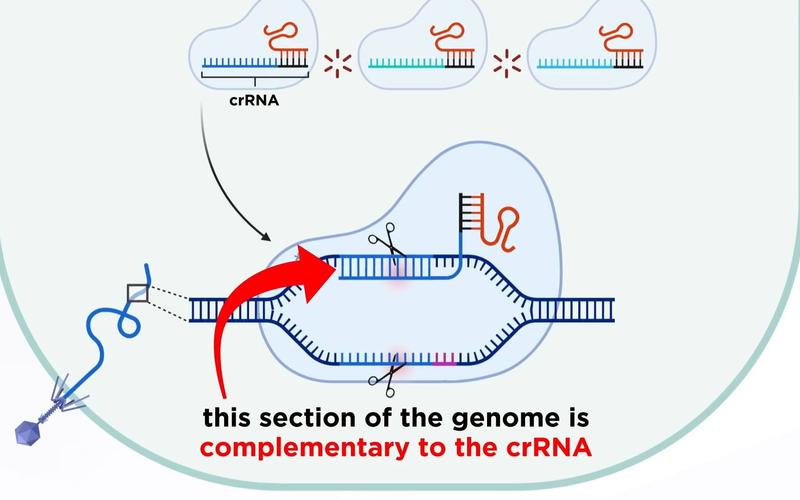
它是一种源于细菌免疫系统的基因编辑工具,细菌用它来“剪掉”入侵的病毒(如噬菌体)的DNA,从而保护自己,科学家们巧妙地“借用”并改造了这套系统,使其成为能够精确切割和修改任何生物(包括人类、植物、动物等)DNA的强大技术。
工作原理:如何找到并“剪切”DNA?
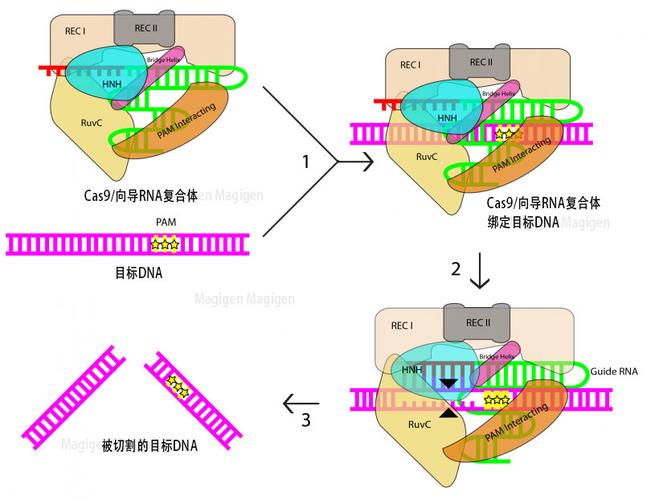
CRISPR-Cas9系统的工作过程可以分为三个核心步骤,非常像一个“GPS导航 + 剪刀”的组合:
导航系统:寻找目标地址
- 向导RNA (Guide RNA, gRNA):这是CRISPR系统的“GPS”,它由两部分组成:
- CRISPR RNA (crRNA):这是一个大约20个碱基长的短序列,它的设计是关键,科学家可以自由设计这个序列,使其与想要编辑的目标DNA序列完全互补。
- 反式激活crRNA (tracrRNA):像一个支架,帮助Cas9蛋白与gRNA结合。
- (在实际应用中,crRNA和tracrRNA常常被设计成一条单链,称为单指导RNA, sgRNA)
- 工作方式:gRNA会带着Cas9蛋白在细胞的DNA长链上“扫描”,一旦它通过碱基互补配对原则,找到了与自身序列完全匹配的目标DNA,就会“停靠”在那里。
剪刀工具:执行剪切
- Cas9蛋白:这是CRISPR系统的“分子剪刀”,它是一种内切酶,专门负责切割DNA。
- 工作方式:一旦gRNA成功定位到目标DNA,Cas9蛋白就会被激活,在目标位点附近进行切割,它通常会在DNA的两条链上各切一刀,形成一个“平末端”的双链断裂。
细胞的修复与编辑:修改基因
当DNA被Cas9剪断后,细胞会启动自身的修复机制,科学家们正是利用了这两种修复机制来实现不同的编辑目的:
-
非同源末端连接
 (图片来源网络,侵删)
(图片来源网络,侵删)- 过程:这是细胞最简单、最快速的修复方式,它会直接将断裂的两端“粗暴”地重新连接起来。
- 结果:在这个过程中,常常会随机地“删除”或“插入”几个碱基,导致基因序列发生移码突变,这通常会使该基因的功能失效。
- 应用:常用于“敲除” (Knockout) 基因,即让某个基因失去功能,从而研究该基因的作用。
-
同源重组修复
- 过程:这是一种更精确的修复方式,细胞会以一份“修复模板” (Donor Template) 为蓝本,来修复断裂的DNA。
- 结果:科学家可以提供一段带有期望修改的DNA序列作为模板,细胞在修复时,会按照这个模板的序列来填补缺口,从而实现基因的“修改”或“替换”。
- 应用:常用于“敲入” (Knock-in),比如修复致病基因突变、插入一个新的基因或给基因加上“标签”。
核心优势:为什么如此革命性?
在CRISPR出现之前,基因编辑技术(如锌指核酸酶TALENs、类转录激活因子效应物核酸酶TALENs)存在诸多限制,CRISPR-Cas9的优势是颠覆性的:
- 简单、快速、成本低:相比于过去需要复杂的蛋白质设计和合成,CRISPR只需要设计和合成一段gRNA,成本极低,周期大大缩短。
- 高效率和高精度:能够在多种细胞类型(包括体细胞、干细胞、受精卵)中实现高效的基因编辑。
- 可编程性:通过简单地改变gRNA的序列,就可以让Cas9蛋白去切割基因组上的任何一个位置,灵活性极高。
- 多靶点编辑:可以同时设计多个gRNA,引导Cas9蛋白在基因组的不同位置进行切割,实现“一石多鸟”的编辑效果。
主要应用领域
CRISPR的应用潜力几乎是无限的,涵盖了多个前沿领域:
医疗健康
- 遗传病治疗:这是最令人期待的应用,理论上,可以修复导致遗传病的基因突变,例如镰状细胞贫血、囊性纤维化、亨廷顿舞蹈症、杜氏肌营养不良症等。
- 癌症免疫疗法:改造患者的T细胞(CAR-T疗法),使其能更精准地识别并攻击癌细胞。
- 传染病防治:通过编辑蚊子基因,使其无法传播疟疾或登革热病毒。
- 药物研发:构建疾病模型细胞系,用于筛选和测试新药。
农业与食品
- 培育抗逆作物:开发能抵抗干旱、盐碱、病虫害的作物,提高产量和安全性。
- 改良食品品质:编辑作物基因,使其更富营养(如富含维生素的“黄金大米”)、储存时间更长、口感更好。
- 提高畜牧业效率:培育生长更快、肉质更优、抗病能力更强的家畜。
基础科学研究
- 基因功能研究:快速“敲除”某个基因,观察生物体或细胞的变化,从而推断该基因的功能。
- 构建疾病模型:在实验动物(如小鼠)中引入特定的人类疾病突变,用于研究疾病机理和治疗方法。
挑战、伦理争议与未来展望
尽管CRISPR潜力巨大,但也面临着严峻的挑战和深刻的伦理问题。
挑战
- 脱靶效应:gRNA可能会错误地结合到非目标但序列相似的DNA位点,导致Cas9在错误的位置进行切割,引发意想不到的基因突变,甚至致癌。
- 递送系统:如何安全、高效地将CRISPR-Cas9系统(通常是巨大的蛋白质和核酸复合物)递送到体内的目标组织和细胞,是一个巨大的技术难题。
- 免疫原性:Cas9蛋白来源于细菌,人体免疫系统可能会将其识别为外来物质并攻击,影响治疗效果。
伦理争议
- 生殖系基因编辑:这是最具争议的领域,指对精子、卵子或早期胚胎的基因进行修改,这些改变会遗传给后代,2025年,中国科学家贺建奎宣布世界首例基因编辑婴儿诞生,引发了全球范围内的强烈谴责和伦理恐慌,主要担忧包括:
- 安全性:脱靶效应等未知风险可能永久引入新的遗传缺陷。
- 社会公平:可能加剧社会不平等,创造出“基因优化”的“设计婴儿”。
- “滑坡效应” (Slippery Slope):一旦打开潘多拉魔盒,未来是否会被用于“增强”人类智力、外貌等非治疗性目的?
- 体细胞基因编辑:指对成体细胞进行编辑,改变不会遗传给后代,目前大多数研究都集中于此,其伦理争议相对较小,但仍需严格监管。
未来展望
- 提高精准度:开发更高级的Cas9变体(如高保真Cas9)和新的编辑工具(如碱基编辑器、质粒编辑器),以减少脱靶效应,实现更精细的修改(如单个碱基的替换,而不需要切断DNA)。
- 递送技术革新:开发更安全、更高效的病毒载体(如AAV)和非病毒载体递送系统。
- 伦理与法规建设:全球科学界和政府正在积极探讨和制定相关的法律法规,确保CRISPR技术在严格的伦理框架内负责任地发展。
CRISPR-Cas9是一项划时代的基因编辑技术,它像一把精准的“基因手术刀”,为我们打开了改造生命、治疗疾病、解决粮食问题的全新大门,这把刀锋利无比,在带来巨大福祉的同时,也伴随着巨大的责任和风险,如何科学、审慎、合乎伦理地使用这项技术,是全人类需要共同面对和思考的重大课题。