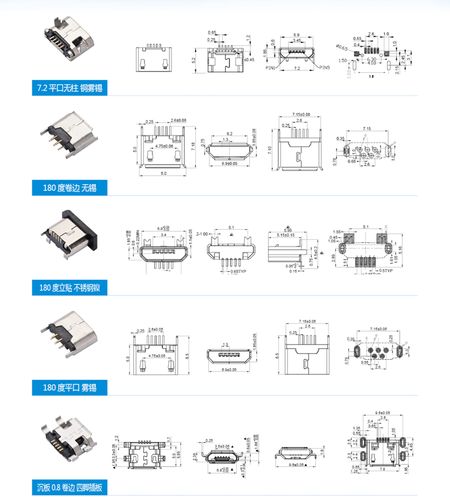
Micro-USB 简介
Micro-USB 是 USB (Universal Serial Bus) 标准家族中的一员,由 USB Implementers Forum (USB-IF) 组织于 2007 年发布,它的主要设计目标是比标准 USB-A 和 Mini-USB 接口更小、更耐用,以适应日益小型化的移动设备。

它主要有两种类型:
- Micro-USB B (Micro-B):最常见的类型,用于大多数安卓手机、移动电源、蓝牙音箱、电子阅读器等。
- Micro-USB AB (Micro-AB):既可以作为主机也可以作为设备,通常用于支持 OTG (On-The-Go) 功能的设备上。
核心技术参数
物理与机械规格
- 接口类型:
- Micro-B:5 针连接器,呈梯形,有防呆设计,不易插反。
- Micro-AB:与 Micro-B 物理兼容,但内部电路设计不同,用于区分主机和设备角色。
- 尺寸:
- 宽度:约 6.8 毫米
- 高度:约 1.8 毫米
- 厚度:约 10 毫米
- 相比 Mini-USB,它更小,连接也更牢固。
- 耐用性:
- 设计标准为可承受 10,000 次插拔。
- 插头有塑料外壳包裹,增强了机械强度和抗弯曲能力。
- 引脚定义 (Micro-B): Micro-USB B 接口有 5 个引脚,其定义如下(从左到右,面对接口正面):
| 引脚编号 | 名称 | 线缆颜色 ( | 功能描述 |
|---|---|---|---|
| 1 | VBUS (电源) | 红 | +5V 电源输入,为设备充电或供电。 |
| 2 | D- (数据负) | 白 | USB 差分信号线负极,用于数据传输。 |
| 3 | D+ (数据正) | 绿 | USB 差分信号线正极,用于数据传输。 |
| 4 | ID | 未连接 (NC) | OTG 关键引脚,用于区分主机和设备。 |
| 5 | GND (地线) | 黑 | 接地,提供电流回路和信号参考。 |
- ID 引脚的作用 (OTG 功能):
- 在支持 OTG 的设备上,Micro-AB 接口通过检测 ID 引脚的电平来判断自身角色。
- ID 引脚接地:设备作为 主机 (Host),可以为 U 盘、鼠标、键盘等外设供电。
- ID 引脚悬空:设备作为 外设 (Peripheral),可以被电脑或其他主机充电或访问数据。
电气规格
- 数据传输速率:
- 遵循 USB 2.0 标准。
- 理论最高速度:480 Mbps (Megabits per second)。
- 实际传输速度:通常在 35-40 MB/s (Megabytes per second) 左右。
- 供电能力:
- 标准 USB 2.0 供电:通过 VBUS 引脚提供 +5V 电压。
- 低功耗设备:最大电流为 500mA (2.5W)。
- 充电专用 (BC - Battery Charging):USB-IF 定义了专门的充电规范,允许更高的电流输出,以加快充电速度,常见的有:
- SDP (Standard Downstream Port):标准端口,最大 500mA。
- DCP (Dedicated Charging Port):专用充电端口(如大部分充电头),可以提供最高 1.5A (7.5W) 或 2A (10W) 的电流,不进行数据通信。
- CDP (Charging Downstream Port):充电下行端口(如大部分电脑 USB-A 口),在数据传输时提供最高 1.5A 的电流,不传输数据时可提供 500mA。
性能总结
| 参数 | 规格 | 备注 |
|---|---|---|
| 技术标准 | USB 2.0 | |
| 接口类型 | Micro-B, Micro-AB | Micro-B 最为常见 |
| 数据速率 | 最高 480 Mbps | 实际约 35-40 MB/s |
| 供电电压 | +5V | |
| 标准电流 | 500mA | 数据传输模式 |
| 充电电流 | 最高 2A (10W) | 充电专用模式,需支持 BC 规范 |
| 物理尺寸 | 宽 6.8mm x 高 1.8mm x 厚 10mm | |
| 插拔寿命 | 10,000 次 | |
| 主要功能 | 充电、数据传输、OTG |
主要应用场景
- 移动设备:安卓智能手机、平板电脑(在 USB-C 普及之前)。
- 移动电源:几乎所有支持 Micro-USB 输入的充电宝。
- 消费电子产品:蓝牙耳机/音箱、电子书阅读器、便携式游戏机、GPS 导航仪等。
- 物联网设备:许多小型嵌入式开发板、传感器模块等。
- OTG 功能:连接 U 盘、鼠标、键盘、游戏手柄等外设到手机或平板上。
优缺点
优点:
- 成熟稳定:技术非常成熟,兼容性好。
- 成本较低:由于大规模使用,制造成本低。
- 体积小巧:比 Mini-USB 更小,适合便携设备。
- 结构坚固:插拔寿命长,连接可靠。
缺点:
- 插入方向性:虽然设计了防呆,但仍需要分正反面插入,不如 USB-C 的盲插方便。
- 速度较慢:仅为 USB 2.0 速度,无法满足高速数据传输需求(如连接高速 SSD 或视频采集卡)。
- 充电功率有限:最高支持 10W,无法满足现代快充协议(如 PD, QC)的高功率需求。
- 接口易损:长期使用后,接口内部的焊点或插座本身容易损坏或松动。
与 USB-C 的对比
随着技术发展,USB-C (Type-C) 已经逐渐取代 Micro-USB,成为新的标准,两者对比非常明显:
| 特性 | Micro-USB | USB-C |
|---|---|---|
| 接口形状 | 梯形,有方向性 | 椭圆形,无方向性(盲插) |
| 数据速率 | 最高 480 Mbps (USB 2.0) | 最高 40 Gbps (USB4 Gen 3x2) |
| 充电功率 | 最高 10W (5V/2A) | 最高 240W (USB PD 3.1) |
| 视频输出 | 不支持 | 支持 DisplayPort, HDMI, Thunderbolt 等协议 |
| 功能扩展 | 功能单一 | 功能强大,可扩展音频、视频、数据等多种功能 |
| 普及程度 | 逐渐被淘汰 | 新设备的主流标准 |
Micro-USB 是一个在移动设备发展史上扮演了重要角色的接口,它以其小巧、坚固、成本低廉的特点,在智能手机和移动电源的普及中发挥了关键作用,由于其在速度、充电功率和便利性上的局限性,它正迅速被功能更强大的 USB-C 接口所取代,尽管如此,由于庞大的存量设备,Micro-USB 仍将在未来一段时间内继续存在和使用。